Você sabia que a “sujeira” do solo pode nos ajudar a vencer a batalha contra as bactérias que nos causam doenças? No início de 2018, pesquisadores da Universidade de Rockfeller, nos Estados Unidos, divulgaram que amostras de solo coletadas por todo o país continham compostos com potencial antimicrobiano, isto é, de combate às bactérias, fungos, protozoários e vírus. O estudo, publicado na revista Nature Microbiology, identificou compostos com capacidade antimicrobiana considerados “naturais”, ou seja, produzidos pelos próprios microrganismos presentes no solo. E não foi só isso, ao analisar as 2.000 amostras de solo, os pesquisadores descobriram uma nova classe de antimicrobianos, que foi chamada de malacidinas.
Muitos anos de estudos ainda serão necessários até que esse novo antimicrobiano seja desenvolvido, testado e aprovado para ser usado como medicamento, mas a sua descoberta poderá auxiliar no combate a algumas bactérias já resistentes à maioria dos medicamentos conhecidos, as chamadas superbactérias. As malacidinas se encaixam na família de antimicrobianos dependentes de cálcio, que agem contra as bactérias ao interferir na sua produção da parede celular e integridade da membrana plasmática. Mas não é assim com todos antimicrobianos.
Como os antimicrobianos atuam?
Esses importantes gladiadores contra bactérias podem ter origem natural, mas os desenvolvidos pelo ser humano em laboratório, ou seja, de origem sintética ou semi-sintética, são os mais comuns. A penicilina, por exemplo, é um antimicrobiano natural secretado pelo fungo Penicillium notatum, acidentalmente descoberta em 1928 por Alexander Fleming – embora haja discordâncias sobre este fato. Mesmo tendo origem natural, a penicilina foi quimicamente modificada e purificada para possibilitar sua comercialização, tornando-se então um composto semi-sintético pelas mãos de Ernst Boris Chain e Howard Walter Florey.
Quando falamos de antimicrobianos estamos tratando de diversos tipos de medicamentos que atuam de diferentes maneiras. Atualmente existem mais de 10 classes de antimicrobianos, as quais estão divididas em inúmeros grupos. Essa grande variedade de fármacos faz-se necessária devido aos diferentes tipos de bactérias e diferentes sítios de infecção, além da tentativa de driblar os diversos tipos de mecanismo de resistência dos microrganismos. Dessa forma, a escolha do antimicrobiano a ser utilizado no tratamento de uma infecção depende de vários fatores.
Tendo em vista que antimicrobianos são fármacos capazes de matar ou inibir o crescimento e o desenvolvimento de microrganismos, é interessante perceber que a essência terapêutica dessas substâncias se baseia na toxicidade seletiva, ou seja, na capacidade de anular o microrganismo causador da doença sem afetar o paciente. Isso é possível devido ao fato dos antimicrobianos interferirem com diferentes atividades da célula bacteriana, interrompendo sua homeostase e seu funcionamento, lembra das malacidinas que interferem na produção da parede e integridade da membrana das células de superbactérias? A seguir estão relacionados os cinco mecanismos de ação dos principais antimicrobianos, e seus respectivos fármacos, para que você saiba mais sobre as formas que podemos vencer essa batalha contra as bactérias (Imagem).
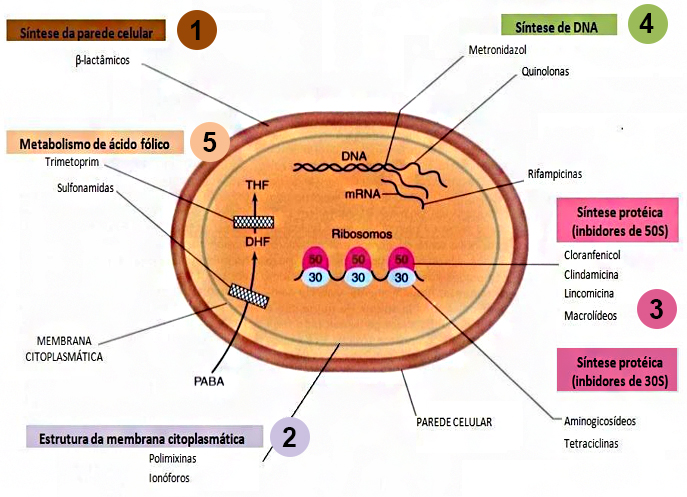 Figura: Relação dos mecanismos de ação dos principais antimicrobianos utilizados no combate às doenças e seus principais fármacos. Imagem: modificado de Pearson Prentice Hall, Inc.
Figura: Relação dos mecanismos de ação dos principais antimicrobianos utilizados no combate às doenças e seus principais fármacos. Imagem: modificado de Pearson Prentice Hall, Inc.
1) Atuação na parede celular
A classe de antimicrobianos β-lactâmicos abrange aqueles com o perfil de atuação mais utilizado na prática clínica. Eles impedem que as bactérias sintetizem sua parede celular através de diversos mecanismos como, por exemplo, a anulação das proteínas ligadoras de penicilina (PBP). Nesse caso, quando utilizamos um β-lactâmico, ele liga-se a uma PBP, deixando essa enzima “ocupada” e incapaz de exercer sua função. Com isso, a síntese da parede celular é interrompida, ocasionando a perda de rigidez dessa parede, e facilitando a quebra da célula bacteriana. Medicamentos como as penicilinas, cefalosporinas, vancomicinas, monobactâmicos e carbapenêmicos estão entre os β-lactâmicos mais conhecidos. Porém, em bactérias desprovidas de parede celular, como os micoplasmas, tais fármacos não possuem efeito algum, por isso, nesses casos, outras estratégias são recomendadas.
2) Ligação à membrana plasmática
Os fármacos que alteram a função e a estrutura da membrana são as polimixinas e os ionóforos. Esses antimicrobianos penetram e se intercalam aos fosfolipídeos da membrana plasmática bacteriana. Com isso, ocorre uma desorganização de sua estrutura e a alteração da sua permeabilidade, ocasionando a saída de componentes celulares e morte da bactéria. Como existem semelhanças entre as membranas citoplasmáticas das bactérias e das nossas próprias células esses antimicrobianos podem apresentar um maior nível de toxicidade, ou seja, também podem destruir células do hospedeiro e causar reações adversas.
3) Interferência na síntese protéica
Alguns antimicrobianos atuam nas duas porções dos ribossomos (30S ou 50S) das bactérias e interferem em diferentes etapas de sua produção de proteínas.
- a) Inibidores de 30S
Aminoglicosídeos (ex: amicacina, tobracina e gentamicina): impedem a leitura correta do código genético, o que leva à produção de proteínas não-funcionais.
Tetraciclinas (ex: tetraciclina e minociclina): não deixam que o RNA transportador se ligue ao ribossomo durante a produção de proteínas.
- b) Inibidores de 50S
Cloranfenicol, clindamicina, lincomicina: esses fármacos interrompem a formação da fita do DNA ao impedir que a enzima peptidil-transferase atue.
Macrolídeos (ex: eritromicina): atuam bloqueando o movimento do ribossomo ao longo do RNA mensageiro.
4) Inibição da síntese de DNA
Essa outra classe de antimicrobianos atua inibindo a síntese de ácidos nucleicos de diferentes maneiras. As rafampicinas ligam-se à enzima RNA polimerase e bloqueiam a transcrição do DNA. Já as quinolonas atuam inibindo a compactação e replicação do DNA. O metronidazol, por sua vez, é degradado dentro da célula pela enzima nitroso-redutase, produzindo produtos tóxicos, os quais geram a quebra da fita do DNA.
5) Interferência no metabolismo de acido fólico
As sulfonamidas e o trimetoprim têm como mecanismo de ação interferir no metabolismo de ácido fólico, elemento importante para a produção de RNA e DNA das bactérias. O trimetoprim é similar ao ácido fólico, ou seja, substitui esse elemento como substrato da enzima diidrofolato redutase e atrapalha o processo. Já as sulfonamidas são similares ao ácido p-aminobenzólico (PABA), que é usado pelas bactérias para a produção do ácido fólico. Assim, o uso da molécula de sulfonamida no lugar da molécula de PABA impede a produção do ácido fólico. O trimetoprim e as sulfonamidas atuam apenas nas bactérias, pois somente esses microrganismos produzem o ácido fólico que irão consumir, diferentemente de animais e seres humanos que precisam ingeri-lo em sua alimentação.
Uma batalha muito importante
Como pudemos ver, essa batalha contra as bactérias não é nada fácil. Aproximadamente 700 mil pessoas morrem a cada ano devido à infecção por bactérias resistentes aos medicamentos existentes, e, até 2050, esse número pode aumentar para até 10 milhões. Portanto, assim como a conscientização sobre a prevenção de doenças e uso adequado de medicamentos, as pesquisas para o desenvolvimento de novos antimicrobianos, como os produzidos nos solos americanos, são de extrema importância pois, no futuro, podem ajudar a salvar muitas vidas.
Ciência et al: Laís Calissi Brisolla Tavares
Fontes consultadas:
Aminov RI. Front Microbiol. 2010; 1: 134.
Trabulsi LR, Alterthum F. Microbiologia. 4.ed. São Paulo: Atheneu, 2008.
Hover BM et al. Culture-independent discovery of the malacidins as calcium-dependent antibiotics with activity against multidrug-resistant Gram-positive pathogens. Nat Microbiol. 2018 3:415-422.
(Editoração: Viviane Santana, Eduardo Borges e Caio Oliveira)

